Composición de Engerix-B
- El principio activo es la cubierta externa del virus de la hepatitis B. Cada dosis contiene 20 microgramos/1 ml de proteína compuesta por esta cubierta externa adsorbida en hidróxido de aluminio hidratado.
- Los demás componentes son cloruro de sodio, fosfato de sodio dihidrato, fosfato de sodio dibásico y agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Engerix-B es un líquido inyectable blanco turbio.
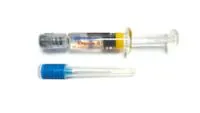
Engerix-B (20 microgramos/ml) está disponible en jeringa precargada de 1 dosis con o sin agujas separadas; tamaños de envase de 1 y 10.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización
GlaxoSmithKline, S.A.
P.T.M. C/ Severo Ochoa, 2
28760 Tres Cantos (Madrid)
Tel.: +34 900 202 700
es-ci@gsk.com
Responsable de la fabricación
GlaxoSmithKline Biologicals S.A.
Rue de l’Institut 89
B-1330 Rixensart
Bélgica
o
SmithKline Beecham, S.A.
Carretera de Ajalvir. Km. 2,5
28806 Alcalá de Henares
Madrid
Este medicamento está autorizado en los Estados miembros del Espacio Económico Europeo con los siguientes nombres:
Austria, Dinamarca, España, Finlandia, Holanda, Islandia, Noruega, Suecia: Engerix-B
Bélgica, Luxemburgo, Portugal: Engerix B
Francia, Irlanda, Italia: Engerix B-20
Alemania: Engerix-B Adult
Grecia: Engerix
Fecha de la última revisión de este prospecto: 02/2024
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/).
---------------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario:
Una vez almacenada, el contenido puede presentarse como un depósito blanco fino con un sobrenadante claro incoloro. Tras la agitación, la vacuna es ligeramente opaca.
Antes de utilizar la vacuna se debe inspeccionar visualmente para detectar partículas extrañas y/o un aspecto físico anormal. No administrar la vacuna si observa cualquiera de los dos.
Debe extraerse todo el contenido del envase monodosis y utilizarse inmediatamente tras la extracción.
Instrucciones para la jeringa precargada
|
    
|
Sostenga la jeringa por el cuerpo, no por el émbolo.
Desenrosque el tapón de la jeringa girándola en sentido contrario a las agujas del reloj.
|
|
 
|
Para insertar la aguja, conecte la base al adaptador luer-lock y gírelo un cuarto de vuelta en el sentido de las agujas del reloj hasta que sienta que se bloquea.
No saque el émbolo de la jeringa del cuerpo. Si esto ocurre, no administre la vacuna.
|
Eliminación de residuos
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.